Coronakrisen og EU’s nye beredskab: Er HERA et kvantespring eller hop fremad?
Da covid-19 krisen ramte Europa i år 2020, havde EU ikke et kriseberedskab, der som i USA kunne håndtere sundhedskrisen. EU grundlagde derfor HERA som et værn mod fremtidige kriser.
RESUME Covid-19-krisen har med al tydelighed vist, at EU manglede et effektivt sundhedskriseberedskab. Modsat USA havde EU ikke et institutionelt set-up eller de nødvendige finansielle midler til at fremskynde udvikling, produktion og indkøb af vacciner. I stedet måtte EU ty til reaktive, ad hoc-løsninger med alt fra indgåelse af vaccinekontrakter til lageropbygning af værnemidler og medicinsk udstyr. EU’s manglende beredskab kostede menneskeliv og medførte en massiv nedlukning af Europas økonomier.
Med inspiration fra USA har EU nu fået en ny myndighed for kriseberedskab og -indsats på sundhedsområdet (HERA), der skal styrke EU’s interne koordination og fællesindsats før og under kriser. I ”fredstid” skal HERA stå for investeringer og tiltag, der sigter på at styrke forebyggelse af og beredskab til nye krisesituationer. I krisesituationer kan HERA hurtigt overgå til at udføre kriseindsatser (så som vaccineindkøb).
Med et samlet system til forberedelse og håndtering af alvorlige grænseoverskridende sundhedstrusler står EU nu stærkere i kampen mod fremtidige sundhedskriser. HERA udgør dog på nuværende tidspunkt næppe et stort nybrud. Flere af problemerne under pandemien er fortsat uløste.
Mest presserende er, at EU stadig ikke har mulighed for at rejse hurtig og massiv kapital i krisetider til at fremskynde vaccineforskning og -udvikling. Paradoksalt nok har EU en reserve til veterinærkriser, men ikke til sundhedskriser der rammer mennesker. Frem mod evalueringen af HERA i 2024 er det derfor vigtigt at have et skarpt øje på netop krisefinansieringen. I hvert fald vil det være et betydeligt legitimitetstab for EU og medlemslandene, hvis europæerne må sande, at EU ikke fremadrettet er bedre rustet til at sikre hurtig adgang til nødvendig medicinske modforanstaltninger (som vacciner og lægemidler).
Indledning
For mig står det krystalklart: Vi skal opbygge en stærkere europæisk sundhedsunion […]. Vi er nødt til at styrke vores kriseberedskab og -styring i forbindelse med grænseoverskridende sundhedstrusler. [Derfor] vil vi opbygge et europæisk BARDA – et agentur for biomedicinsk avanceret forskning og udvikling
Sådan lød ordene fra kommissionsformand Ursula von der Leyen i september 2020 i sin årlige tale om Unionens tilstand med direkte reference til det amerikanske pandemiagentur, BARDA. Kommissionsformanden ambitioner fejlede ikke noget. EU måtte tage ved lære af sine fejl af ikke at have opbygget og investeret i en fælles beredskabs- og indsatskapacitet til at reagere hurtigt og koordineret på alvorlige grænseoverskridende sundhedstrusler.
Da Covid-19-pandemien ramte Europa i starten af 2020, havde EU ikke en værktøjskasse parat til at håndtere krisen – og medlemslandene var lige så uforberedte på nationalt plan. EU havde intet overblik over udbuddet af og produktionskapaciteten for medicinske modforanstaltninger, så som værnemidler og respiratorer, endsige antallet af intensivpladser på medlemsstaters hospitaler. Der var heller ingen strategiske lagrer for farmaceutiske produkter at trække på, da de globale forsyningskæder svigtede i starten af krisen. F.eks. leverede Kina langt fra alle de værnemidler, Europa havde brug for. Og da det stod klart, at Covid-19 kun kunne bekæmpes med vacciner, manglede EU den nødvendige struktur til at støtte udvikling, produktion og indkøb af vacciner. Det er ikke overraskende, da sundhed er national kompetence, men krisens grænseoversskridende karakter bevirkede, at EU havde store problemer med og behov for at udvikle fællessvar.
EU’s situation stod i skærende kontrast til situationen i USA. Det amerikanske agentur for biomedicinsk avanceret forskning og udvikling (BARDA) var grunden til, at amerikanerne fik hurtigere adgang til Covid-19-vacciner end europæerne2 . Opskriften var mangeårige, massive investeringer i vaccineforskning og -udvikling knyttet til forhåndsindkøbsaftaler samt stærke offentlig-private partnerskaber. Det var også BARDA, der med et øget budget under Covid-19-krisen indgik vaccinekontrakter med de vaccineproducenter, de støttede.
For Europa-Kommissionen stod det hurtigt klart: EU måtte have sit eget BARDA-lignende set-up. Der gik et år fra ord til handling. Samme dag som von der Leyens 2021-tale om Unionens tilstand i september 2021 præsenterede Kommissionen forslaget til EU’s pendant: en myndighed for kriseberedskab og -indsats på sundhedsområdet (HERA).
HERA indgår som en vigtig del af oprettelsen af en europæisk sundhedsunion, der også inkluderer en styrkelse af den retlige ramme for grænseoverskridende sundhedstrusler, en lægemiddelstrategi for Europa og et udvidet og forbedret mandat til både Det Europæiske Lægemiddelagentur (EMA) og Det Europæiske Center for Forebyggelse og Kontrol med Sygdomme (ECDC)3 .
HERA skal sikre forsyning af og adgang til medicinske modforanstaltninger, såsom vacciner, lægemidler, medicinsk udstyr og diagnostik, der indtil nu har været opdelt mellem flere af EU’s politiske rammer og finansieringsprogrammer. HERA’s indsatsområde er todelt: (1) Beredskab før en krise beskrevet i en meddelelse og (2) indsatsen under en krise udbygget i en rådsforordning, vedtaget af Rådet d. 20. december 2021.
Kommissionens HERA-udspil i september 2021 fik en blandet modtagelse. Mediet Politico konkluderede, at ”HERA ikke var den helt, som Europa-Parlamentet havde håbet på, men heller ikke den nytænkning Rådet havde frygtet”4 . Kommissionens ambitioner om at oprette et europæisk BARDA var da også nedskaleret. Som udtrykt af næstformand for Kommissionen, Margaritis Schinas, ”Vi ønsker ikke at øge forventningerne og give indtrykket af, at det her er en game-changer […]. Men vi mener, at det er en ny struktur med en klar merværdi”5 . Særligt Europa-Parlamentet (EP) var skuffede over, at HERA ikke blev oprettet som et selvstændigt agentur, som Kommissionen oprindeligt havde lagt op til, og dermed satte Parlamentet uden for indflydelse.
I dette notat ser Tænketanken EUROPA nærmere på, hvordan HERA bidrager til at højne EU’s sundhedskriseberedskab og -indsats fremadrettet. Hvad har EU lært af krisen, og i hvor stort omfang vil man stå bedre, hvis eller måske snarere når en ny krise rammer på ny. Notatet giver først et overblik over de forsyningsvanskeligheder, EU stod over for under pandemien – og de ad hoc-foranstaltninger EU anvendte for at afhjælpe dem. Herefter ser vi nærmere på HERA’s tiltænkte rolle i beredskabs- og krisefasen samt udfordringerne med HERA’s nuværende set-up.
Notatet bygger både på input fra 10 interviews med medicinalindustrien, nationale og EU-embedsmænd og forskere samt et roundtable om ”HERA’s fremtidige rolle” afholdt i november 2021 af Tænketanken EUROPA i samarbejde med Lægemiddelindustriforeningen (Lif).
Overblik: EU’s ad hoc-løsninger under pandemien
Covid-19 pandemien satte globale forsyningskæder under pres. På sundhedsområdet førte den kraftige stigning i efterspørgslen efter sundhedsforsyninger til mangel på lægemidler, respiratorer, mundbind, test- og laboratorieudstyr samt materialer og ingredienser til vaccineproduktion. EU’s beskedne krisestrukturer og medlemslandenes ringe forberedelse bevirkede, at EU og medlemslandene måtte improvisere sig igennem krisen og udvikle krisesvar, mens krisen løbende tog fart6 . EU tyede til en række ad hoc-løsninger for at adressere manglen på kritiske forsyninger, der nu alle er blevet en integreret del af HERA:
- Indkøb og oplagring af personlige værnemidler gennem oprettelsen af ti EU-finansieret lagre (rescEU).
- En clearingcentral for medicinsk udstyr til at matche udbud og efterspørgsel i EU af kritisk medicinsk udstyr (så som respiratorer) og sikre hurtig levering af udstyret.
- EU’s vaccinestrategi7 , vedtaget i juni 2020, for at fremskynde udvikling, fremstilling og anvendelse af Covid-19-vacciner. Strategien sikrede EU-landene rettidig og lige adgang til effektive og sikre vacciner til en økonomisk overkommelig pris. EU blev under pandemien kritiseret for at have sovet i timen og indkøbt for lidt og forkert ind af vacciner ved at insistere for meget på at få en lavere pris per vaccinedosis. Det betød, at EU fik leveret sine vaccinedoser senere end de lande, der var villige til at betale mere, hvilket forlængede nedlukningen af den europæiske økonomi.
- Europa-Kommissionen oprettede i februar 2021 taskforcen for industriel opskalering8 ledet af kommissæren for det indre marked, Thierry Breton. Taskforcens formål er at øge vaccineproduktionskapaciteten i EU ved at fungere som kvikskranke for vaccineproducenter og aktører i forsyningskæden, som har behov for hjælp til at identificere og afhjælpe flaskehalse i produktionskapaciteten og forsyningskæderne for vacciner. Det betyder, at Kommissionen i dag har et godt kendskab til produktionskapaciteten for vacciner i EU.
- HERA Incubator, oprettet i februar 2021, imødegår trusler fra nye Covid-19 varianter ved at overvåge mutationer, fremskynde produktion og godkendelse af tilpassede vacciner. Samarbejdet bygger på et offentligt-privat partnerskab mellem forskere, bioteknologiske virksomheder, producenter og offentlige myndigheder9 .
- ”Vaccelerate”, lanceret i februar 2021, er det første EU-netværk for kliniske forsøg med Covid-19-vacciner og indgår som led i HERA Incubator. Netværket skal gøre samarbejde og datadeling under kliniske forsøg med Covid-19-vacciner og -behandlinger nemmere.
- "EU FAB"-projektet, også søsat i februar 2021, er et netværk af beredskabsproduktionskapaciteter til fremstilling af vacciner og lægemidler i EU. Det skal sikre et "konstant varmt" netværk af medicinalproduktion, der hurtigt kan øge produktionen af vacciner og lægemidler i fremtidige sundhedskriser.
Listen af EU-tiltag under pandemien til at adressere en række af de forsyningsvanskeligheder, EU og resten af verdenen oplevede under pandemien, er på mange måder imponerede. Fælles for dem alle er, at de var reaktive og ad hoc-løsninger, der kostede EU dyrebar tid, menneskeliv og økonomiske tab. Pandemien gjorde det klart, at EU har brug for pro-aktive og strukturelle svar på fremtidige sundhedskriser. Pandemien har vist nødvendigheden af at overvåge og forme markedet og kapaciteter for sundhedsforsyninger i alle faser – fra forskning og udvikling til produktion og forsyning. Det er netop her, at etableringen af HERA udfylder et hul i EU’s kriseberedskab og -indsats.
HERA i ”fredstid”
HERA blev etableret gennem en Kommissionsafgørelse10 d. 16. september 2021, som en ny, permanent og intern struktur i Kommissionen. Kommissionen har derfor selv bestemt, hvordan HERA rent praktisk er opbygget efter høring af interessenter og medlemslandene. Hverken Rådet eller EP har haft direkte mulighed for at påvirke forankringen og organiseringen af HERA i beredskabsfasen. Med sundhedskommissæren Stella Kyriades egne ord er, ”tid hovedårsagen til, at Kommissionen ikke foreslog at gøre HERA til et selvstændigt agentur. Derimod sikrer en intern kommissionsstruktur, at HERA er operationel med det samme og har adgang til de nødvendige finansielle og menneskelige ressourcer tilgængelige i Kommissionen. Et agentur ville have taget flere år at etablere og ville formentlig ikke have haft de kompetencer og den agilitet, Kommissionens tjenestegrene har. Det handler ikke om at ekskludere [Rådet og EP], men om at handle hurtigt” 11 .
Det spillede uden tvivl også ind, at oprettelsen af et agentur ville have udløst et tidskrævende opgør om, hvor agenturet skulle placeres. Da coronaen stadig var over Europa talte meget for en pragmatisk løsning, hvor EU fik placeret HERA hurtigt.
Oprettelsen af HERA som et decentralt EU-agentur ville have givet både Rådet og EP direkte indflydelse på HERA’s opbygning og kompetencer. Et agentur havde også givet EP formel demokratisk kontrol med HERA gennem regelmæssige høringer og afrapporteringsforpligtelser til EP. Typisk er nyudpegede direktører for EU’s agenturer forpligtet til at stille op til høring i EP, før de formelt kan tiltræde deres stilling. EU’s sundhedskommissær forsikrede dog parlamentarikerne under en høring i EP i september 2021 om, at Parlamentet vil være repræsenteret i både HERA’s bestyrelse i beredskabs- og krisefasen og blive holdt fuldt ud informeret12 . Derimod ville et agentur have været mere uafhængig af Kommissionen og have haft sit eget – og formentlig større – budget samt flere ansatte.
Mission og opgaver i fredstid
HERA arbejder tæt sammen med andre EU-agenturer og nationale sundhedsagenturer, erhvervslivet og internationale partnere for at forbedre EU's beredskab og indsats over for alvorlige grænseoverskridende trusler inden for medicinske modforanstaltninger. HERA’s mission er trefoldig. For første skal HERA styrke koordinering af sundhedssikkerheden i EU, når det gælder beredskab, kriseresponstider og samle medlemslandene, erhvervslivet og andre relevante aktører i en fællesindsats. For det andet skal HERA mindske EU’s sårbarheder og afhængighed i forhold til udvikling, fremstilling, indkøb, lageropbygning og distribution af medicinske modforanstaltninger. For det tredje skal HERA være med til at styrke den globale struktur for kriseberedskab og – indsats på sundhedsområdet ved blandt andet at sikre et tæt samarbejde med globale partnere for at afhjælpe internationale flaskehalse i forsyningskæden, fjerne restriktioner og udvide den globale produktionskapacitet.
HERA skal også gennem Verdenssundhedsorganisationen (WHO) være med til at styrke den globale overvågning af sundhedstrusler. Derudover vil EU gennem HERA fortsætte med at støtte tredjelandes adgang til EU-finansierede eller -indkøbte medicinske modforanstaltninger og bistå lav- og mellemindkomstlande med at opbygge ekspertise og produktionskapacitet på området. For at efterleve sine tre missioner skal HERA varetage seks typer af opgaver i beredskabsfasen:
- Vurdering af sundhedstrusler og indsamling af efterretninger der er relevante for medicinske modforanstaltninger. Fokusområdet er trusler forårsaget af biologiske, kemiske eller miljømæssige faktorer – uanset om de opstår naturligt, ved uheld eller forsætligt (tekstboks 1 viser de trusler, HERA har fokus på lige nu). HERA har kapaciteter til horisontafsøgning, fremsyn, dataanalyse, markedsmæssige efterretninger samt løbende udveksling med nationale eksperter med henblik på udarbejdelse af fællesanalyser. HERA styrker medlemslandenes kapacitet til at foretage genomsekventering (dvs. kortlægning af patienters arvemasse) og miljøovervågning, så som overvågning af spildevand og etablering af effektive dataudvekslingsplatforme, herunder det fremtidige europæiske sundhedsdataområde.
- Støtte avanceret forskning og udvikling (R&D) af medicinske modforanstaltninger og teknologier, herunder diagnostik, behandlinger og vacciner. Europæiske netværk og platforme til hurtig udveksling af data for kliniske forsøg med vacciner og behandlinger (så som ”Vaccelerate”) skal fremskynde forsøg og forbinde relevante aktører i forbindelse med udførelsen af forsøgene. Disse platforme skal nemt kunne tilpasses et bredt spektrum af trusler for at afkorte produktions- og leveringstider. HERA formulerer en fælles EU-forsknings- og innovationsdagsorden for pandemiberedskab, understøttet af både EU og national finansiering og gør brug af det planlagte ”vigtige sundsprojekt af fælleseuropæisk interesse” (IPCEI på sundhedsområdet13 ) samt samler fragmenterede forskningskapaciteter på området.
- Håndtering af markedsmæssige udfordringer og en styrkelse af EU’s åbne strategiske autonomi inden for produktion af medicinske modforanstaltninger. HERA identificerer og sikrer tilgængeligheden af kritiske teknologier og produktionsanlæg for medicinske modforanstaltninger i EU med kapacitet til at øge produktionen efter behov (jf. ”EU FAB”). HERA hjælper med at styrke erhvervslivets modstandsdygtighed i EU for udefrakommende chok gennem langsigtede investeringer, planlægning og offentlig-privat partnerskaber. Større EU-koordination skal sikre, at EU ikke er for afhængig af forsyninger uden for Europa gennem opbygning af robuste forsyningskæder og udvidelse af medlemslandenes produktionskapacitet.
- Sikring af forsyninger af medicinske modforanstaltninger gennem lageropbygning, EU offentlige indkøb og distribution. Rationalet bag EU’s vaccinestrategi – udviklet af Kommissionen og medlemslandene som et ad hoc-redskab under pandemien – skal tjene som forbillede for fremtidige offentlige indkøb. HERA gør udvikling og indkøb af vacciner og andre medicinske modforanstaltninger en del af samme udbudsprocedure.
- Udbredelse af kundskaber og færdigheder inden for beredskab og indsats i medlemslandene. HERA vil tilrettelægge uddannelsesprogrammer for at forbedre ekspertise i forhold til at sikre adgang til relevante medicinske modforanstaltninger.
- Internationalt engagement for at sikre tilgængelighed og adgang til medicinske modforanstaltninger for EU og tredjelande i sundhedskriser. Det sker gennem et tæt samarbejde med globale partnere (så som WHO) for at adressere globale flaskehalse i forsyningskæderne, fjerne unødvendige restriktioner og udvide den globale produktionskapacitet. HERA skal fremme informations-, videns- og datadeling for at forbedre adgangen til og udviklingen af medicinske modforanstaltninger samt foretage trusselsvurderinger, overvågning og kapacitetsopbygning i tredjelande.


HERA's mandat er rettet mod sundhedskriser og forsyninger af og adgang til medicinske modforanstaltninger. HERA kommer til at arbejde tæt sammen med EMA og ECDC og supplerer deres arbejde under og forud for krisesituationer på områder som kliniske forsøg, beredskabs- og indsatsplanlægning og indsamling af efterretninger. Hverken ECDC eller EMA har mandat til indkøb, udvikling og fremstilling af medicinske modforanstaltninger. ECDC’s mandat er begrænset til trusler fra overførbare sygdomme og har ikke mandat inden for andre sundhedstrusler. EMA er ansvarlig for videnskabelig evaluering, overvågning og sikkerhedskontrol af lægemidler i EU – og ikke andre medicinske modforanstaltninger. HERA vil derfor have enekompetence i forhold til udvikling, produktion, indkøb og distribution af medicinske modforanstaltninger.
Organisation og finansieringsstruktur i fredstid
HERA er etableret som et selvstændigt generaldirektorat (DG) i Kommissionen på lige fod med andre DG’er. Målet er, at HERA i slutningen af 2023 har 120 fuldtidsfastansatte, der bliver rekrutteret både internt og eksternt i Kommissionen. Lige nu har HERA. ca. 60 ansatte.
HERA er i beredskabsfasen ledet af en bestyrelse, der består af Kommissionen og en højtstående repræsentant på embedsmandsniveau fra hvert medlemslands sundhedsministerium, der mødes mindst fire gange om året. Det er op til de enkelte medlemslande at vælge deres repræsentant - samt hvilket ”niveau” repræsentanten er på. HERA’s chef er formand for bestyrelsen og har status som generaldirektør i Kommissionen. Europa-Parlamentet har en repræsentant som observatør. Bestyrelsen bistår og rådgiver Kommissionen om 1) forslag til de aktiviteter, HERA gennemfører som led i sine seks opgaver og evt. nye opgaver, 2) aktiviteternes sammenhæng med andre EU-programmer, 3) den flerårige strategiske planlægning og 4) forslag til det årlige budget og overvågningen af dets gennemførelse.
HERA har desuden et rådgivende forum, der skal sikre et tæt samarbejde mellem HERA og medlemslandenes kompetente organer om planlægning og gennemførelse af HERA’s videnskabelige, sundheds- og produktionsmæssige aktiviteter. Det består af repræsentanter fra nationale teknisk-kompetente organer, der ikke samtidig er medlemmer af bestyrelsen. Det rådgivende organ er stadig under konstruktion.
HERA’s bestyrelse kan oprette undergrupper under det rådgivende forum for at undersøge konkrete spørgsmål inden for videnskab, forskning og fremstilling. Der bliver også etableret et fælles samarbejdsforum med deltagelse af repræsentanter fra erhvervslivet i starten af 2022. Samarbejdsforummet skal hjælpe med at identificere flaskehalse og markedsfejl i og uden for EU, der kan reducere produktionskapaciteten af medicinske modforanstaltninger og råvarer under en sundhedskrise – og afrapportere deres konklusioner i en rapport.
HERA's aktiviteter har et budget på €6 milliarder (svarende til ca. 44,6 mia. kroner) for perioden 2022-2027 fra den nuværende flerårige finansielle ramme. Midlerne kommer fra eksisterende kilder på EU-budgettet, herunder EU4Health (EU’s sundhedsbudget), rescEU (EU-lagre for værnemidler og medicinsk udstyr), NextGenerationEU (EU’s midlertidige genopretningsinstrument) og Horizon Europe (EU’s forskningsbudget). Over halvdelen af EU4Health-budgettet er øremærket til HERA. Tabel 1 viser HERA’s planlagte budget for 2022 og fordelingen mellem HERA’s seks opgaver.
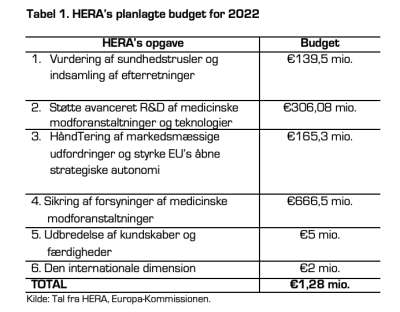
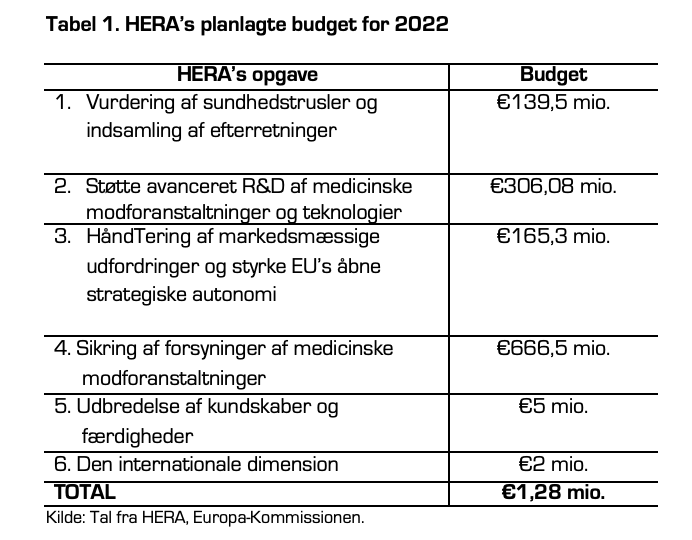
HERA’s årlige bevilling i fredstid svarer nogenlunde til det, BARDA får. Siden BARDA blev etableret i 2006 som et agentur under det amerikanske sundhedsministerium, har det årligt fået bevilliget $1,6 mia.
HERA i krisetid
I slutningen af december 2021 vedtog Rådet en rådsforordning om en ramme for tiltag, der skal sikre forsyning af kriserelevante medicinske modforanstaltninger i tilfælde af en folkesundhedsmæssig krisesituation på EU-plan14 Kommissionen vil med den kommende, reviderede forordning om alvorlige grænseoverskridende sundhedstrusler15 selv kunne udråbe folkesundhedsmæssige krisesituationer på EU-plan, der aktiverer EU’s krisemekanismer til håndtering af sundhedskriser.
Forslaget om sundhedstrusselsforordningen lægger op til, at Kommissionen nedsætter et uafhængigt rådgivende udvalg (bestående af uafhængige eksperter samt repræsentanter fra ECDC, EMA, HERA og andre EU-instanser som aktører), der skal bidrage med ekspertise om, hvorvidt en trussel udgør en folkesundhedsmæssig krise på EU-plan. Det betyder, at EU ikke længere er afhængig af, at WHO erklærer en folkesundhedsmæssig krisesituation, om end Kommissionen skal holde WHO underrettet.
Krisestyring: Who calls the shots?
I tilfælde af anerkendelsen af en folkesundhedsmæssig krisesituation kan Rådet med kvalificeret flertal og efter indstilling fra Kommissionen lade HERA overgå til ”krisetilstand” og aktivere HERA’s nødhjælpsramme. Sker det, overgår styringen af HERA til en sundhedskrisebestyrelse, der skal sikre EU-koordination af kriserelevante medicinske modforanstaltninger.
Formandskabet af sundhedskrisebestyrelsen er delt mellem Kommissionen og Rådets roterende formandskab. Hvert medlemsland nominerer en repræsentant og suppleant til bestyrelsen på embedsmandsniveau. Rådet fik taget ud af teksten, at det skulle være en ”senior official”. Det betyder, at medlemslandenes repræsentanter ikke nødvendigvis behøver at være en højtstående embedsmand. Det er endnu uklart, om repræsentanterne her kan være de samme som i HERA’s bestyrelse i fredstid, da det stadig mangler at blive fastlagt.
Det todelte formandskab skal sikre deltagelsen af andre relevante EU-institutioner og -organer som observatører, herunder ECDC og EMA, en repræsentant fra EP og sundhedssikkerhedsudvalget16 og hvor relevant en repræsentant fra WHO. Sundhedskrisebestyrelse skal sørge for informationsudveksling med EU’s integrerede mekanisme for politisk kriserespons (IPCR). IPCR understøtter hurtig og koordineret beslutningstagning på EU’s politiske niveau i store og komplekse kriser (som f.eks. Covid-19-pandemien eller terrorhandlinger) gennem koordination fra Rådets formandskab. Derfor er det også en fordel for HERA, at Rådets formandskab nu også deler formandskabet af HERA for at højne koordinationen mellem Rådet og Kommissionen. Det er endnu ikke fastlagt, hvem Kommissionen er repræsenteret af i krisebestyrelsen.
Kommissionen skal sørge for et konstant informationsudveksling til bestyrelsen om planlagte og gennemførte tiltag. Når det er muligt, skal Kommissionen konsultere bestyrelsen i god tid, før Kommissionen træffer beslutninger om relevante tiltag og sørge for at tage drøftelserne i bestyrelsen med i sine overvejelser samt rapportere tilbage til bestyrelsen om gennemførte tiltag. Kommissionen skal give en begrundelse til medlemslandene, hvis Kommissionen ikke følger deres forslag. Bestyrelsen skal stile efter at opnå konsensus under sine drøftelser, og hvis det ikke kan lade sig gøre, træffer bestyrelsen beslutninger med flertal med to tredjedele af de nationale repræsentanter, hvor hvert medlemsland har en stemme.
Bestyrelsen er fra Kommissionens side blevet mindre top-styret i det endelige set-up, da Rådet i den endelige tekst fik slettet, at kommissionsformanden, sundhedskommissæren og andre relevante kommissærer repræsenterer Kommissionen i bestyrelsen. I stedet vil Kommissionen være repræsenteret af en embedsmand, der – ifølge Rådet – er et mere passende og tilsvarende niveau med medlemslandenes repræsentanter. Som udtalt af en anonym interviewperson i Rådet: ”Hvis Rådet skulle matche Kommissionens forslag om at have kommissærer repræsenteret i bestyrelsen, ville det svarer til, at Rådet skulle være repræsenteret med sine ministre eller regeringschefer – og det ville ikke være en passende brug af ressourcerne eller meningen med HERA”17 .
Medlemslandenes rolle i sundhedskrisebestyrelsen var et af de store stridsspørgsmål mellem Rådet og Kommissionen i forhandlingerne om rådsforordningen om HERA’s krisekompetencer. Flere medlemslande var skeptiske over for Kommissionens udspil, hvor Kommissionen alene stod for formandskabet af bestyrelsen og ikke havde de samme forpligtelser som nu til at konsultere og informere medlemslandenes repræsentanter både før og efter, Kommissionen træffer beslutninger.
Det er på nuværende tidspunkt tvivlsomt, hvad medlemslandenes nu større rolle i sundhedskrisebestyrelsen kommer til at betyde for Kommissionens fleksibilitet og spillerum. Meget afhænger af, hvordan det kommer til at ske i praksis. En central embedsmand i Kommissionen svarer, at ”det også kan være en fordel at have rådsformandskabet med i bestyrelsens ledelse, da medlemslande har en anden og mere direkte kontakt til hinanden, end Kommissionen har – og nogle gange bedre kan lægge pres på hinanden og få ting til at ske. Derudover giver det medlemslandene større ejerskab, at de har en repræsentant i ledelse”18 . Det er dog samtidig vurderingen i Kommissionen og Rådet, at når det virkelig skal gå stærkt i en krisesituation, kan Kommissionen lave en lynspørgerunde i bestyrelsen og forklare sine planer og handlinger.
EU’s vaccinestyringsudvalg har et lignende set-up, da der også her er delt ledelse mellem Kommissionen og Rådet. Under pandemien førte Kommissionen sammen med et fælles forhandlingsteam forhandlingerne med vaccineleverandørerne. Styringsudvalget udpegede det fælles forhandlingsteam, der repræsenterede syv EU-lande (Frankrig, Tyskland, Italien, Polen, Spanien, Sverige og Holland). Vaccinestyringsudvalget bliver nu videreført i HERA-regi med et lignende set-up. Netop det forhold, at alle medlemsstaterne skulle give deres besyv med skabte en træg beslutningsproces, som HERA også risikerer at løbe ind i. En af vaccineproducenterne fremførte for eksempel, at virksomheden i sommeren 2020 reelt forhandlede med 27 lande, da Kommissionen var ret fastlåst i sit mandat og hele tiden skulle vende tilbage til medlemslandene. I modsætning havde Storbritannien og USA et langt smallere set-up.
Værktøjskassen under sundhedskriser
I en krisesituation kan Rådet efter forslag fra Kommissionen aktivere seks krisemekanismer med kvalificeret flertal enten uafhængigt af hinanden eller samtidigt, hvoraf en række af dem kræver, at sundhedskrisebestyrelsen har været konsulteret:
- Monitorering af kriserelevante medicinske modforanstaltninger (artikel 6): Kommissionen skal efter rådgivning fra sundhedskrisebestyrelsen regelmæssigt opdatere en liste over kriserelevante medicinske modforanstaltninger og råmaterialer samt udarbejde en skabelon for overvågning af udbud og efterspørgsel, herunder produktionskapacitet, lagerføring, indkøbsaftaler og risiko for forsyningssvigt.
- Udbud, indkøb og produktion af kriserelevante medicinske modforanstaltninger og rådmaterialer (artikel 7): Medlemslandene kan give Kommissionen mandat til at agere som et centralt indkøbsorgan på deres vegne gennem aktivering af eksisterende kontrakter eller forhandling af nye. Kommissionen skal i tæt koordination med sundhedskrisebestyrelsen udarbejde et forslag til en rammeaftale, som deltagende medlemslande underskriver. Rammeaftalen skal inkludere proceduremæssige regler for iværksættelsen og forberedelsen af indkøbsproceduren, betingelser og tidsfrister for medlemslandenes deltagelse, involveringen af de deltagende lande i indkøbsprocessen samt fordelingsproceduren af indkøbte medicinske modforanstaltninger. Medlemslandene bestemmer selv, om de vil deltage inden for en aftalt tidsfrist. Kommissionen skal regelmæssigt informere bestyrelsen om fremskridtene i indkøbsproceduren og substansen af forhandlingerne med økonomiske aktører. Kommissionen skal kun starte eventuelle forhandlinger, når et ”tilstrækkeligt” antal medlemslande har udtrykt deres opbakning. Det er endnu ikke defineret, hvor mange lande det kræver. Deltagende medlemslande skal have mulighed for at kommentere på alle kontraktudkast, før forhandlinger med økonomiske aktører bliver afsluttet.
- Aktivering af forsknings-, innovations- og datadelingsplatforme samt anvendelsen af netværk for kliniske forsøg (artikel 8): Kommissionen skal efter rådgivning fra sundhedskrisebestyrelsen støtte adgangen til relevant data fra kliniske forsøg og real-world data samt inddrage EMA.
- Inventarlister for produktionen og produktionsfaciliteter til medicinske modforanstaltninger samt råmateriale, forbrugsvarer, udstyr og infrastruktur (artikel 9 og 10): Kommissionen kan ved brug af gennemførelsesretsakter udarbejde og regelmæssigt opdatere inventarlisterne. Kommissionen kan anmode producenter af medicinske modforanstaltninger om inden for fem dage at informere Kommissionen om deres aktuelle samlede produktionskapacitet og -faciliteter samt lagerbeholdning af kriserelevante medicinske modforanstaltninger i EU- og tredjelande. Kommissionen skal regelmæssigt informere EP og Rådet om lagre, produktion og forventet produktionsrate af medicinske modforanstaltninger i EU samt forsyninger fra produktionsfaciliteter i tredjelande.
- Sikring af tilgængeligheden af medicinske modforanstaltninger (artikel 11): Hvis Kommissionen vurderer, at der er risiko for forsyningsudfordringer med kriserelevante medicinske modforanstaltninger, kan Kommissionen omlægge værdikæder, produktionslinjer, tage eksisterende lagre i brug for at øge forsyningen af kriserelevante medicinske modforanstaltninger hurtigst muligt. Det sker efter aftale med medlemslandene og efter samråd med de berørte økonomiske aktører.
- Aktivering af nødfinansiering (artikel 12): Kommissionen kan gøre brug af nødhjælpsinstrumentet19 (ESI, ”emergency support instrument”) til at finansiere udgifter forbundet med folkesundhedsmæssige krisesituationer, så som forhåndsindkøbsaftaler med vaccineproducenter.
De seks ovenstående krisemekanismer kan aktiveres i op til seks måneder med mulighed for forlængelse.
Forordningen har hjemmel i artikel 122 stk. 1 i Traktaten om Den Europæiske Unions funktionsmåde (TEUF) om vedtagelse af foranstaltninger i tilfælde af vanskeligheder i et medlemsland, typisk energiforsyningsvanskeligheder – og ikke den generelle hjemmel om folkesundhed (TEUF-artikel 168), som Kommissionen ellers havde lagt op til i sin indledende konsekvensanalyse.20 Artikel 122 TEUF har allerede været brugt før under coronakrisen til at oprette SURE med, der er et EU-instrument for midlertidig støtte til mindskelse af risiciene for arbejdsløshed i en nødsituation som følge af covid-19-udbruddet
Modsat artikel 168, sikrer artikel 122, at EU kan give økonomisk assistance til medlemslande, hvis et eller flere medlemslande kommer i alvorlige forsyningsvanskeligheder. Artikel 168 handler udelukkende om koordination og gør det ikke muligt for EU at ty til nødsfinansiering. Det var afgørende for Kommissionens beslutning om ikke at gøre brug af artikel 168.
Hjemlen stiller dog EP uden for formel indflydelse, da det er Rådet, der udelukkende træffer afgørelse med kvalificeret flertal på forslag af Kommissionen. EP har været særdeles utilfredse med at blive hægtet af og har gennem forhandlingerne om at revidere forordningen om alvorlige grænseoverskridende sundhedstrusler21 forsøgt indirekte at sætte sine fingeraftryk på HERA’s rolle i både beredskabs- og krisefasen – dog tilsyneladende uden succes. EP har særligt slået på gennemsigtighed i HERA’s offentlige investeringer i forskning, udvikling, produktion, indkøb, lagring, udbud og fordeling af medicinske modforanstaltninger, samt at fælles indkøbsprocedurer skal være gennemsigtig. Disse elementer er ikke med i den endelige politiske enighed om HERA’s nødhjælpsramme i krisetider.
Er HERA tilstrækkelig?
HERA er stadig work-in-progress og endnu ikke fuldt ud operationel. Tiden vil derfor vise, hvor effektivt HERA kommer til at køre i praksis. Der er dog en række udfordringer med HERA’s nuværende struktur, der ikke tilstrækkeligt lukker hullerne i EU’s kriseberedskab. Det drejer sig om HERA’s budget, ”bureaukratiske funktion”, investeringer, lageropbygning, inddragelse af industrien og adgangen til fyldestgørende og rettidigt data.
For det første er det værd at hæfte sig ved, at nødhjælpsinstrumentet ikke har sit eget budget – og derfor har EU ikke et dedikeret krisebudget. Det betyder, at Kommissionen hver gang der opstår en sundhedskrise, først skal undersøge, om der kan overføres midler fra andre eksisterende programmer, specielle instrumenter eller medlemslandene.
Nødhjælpsinstrumentet blev brugt under pandemien til at finansiere fremstilling af Covid-19-vacciner gennem forhåndsaftaler med vaccineproducenter med et beløb på €2,7 mia. til at dække de indledende omkostninger.22 Til sammenligning etablerede den amerikanske regering det offentlige-private partnerskab, Operation Warp Speed (OWS) for at fremskynde udvikling, produktion og distribution af Covid-19-vacciner. Den amerikanske kongres bevilligede i alt $18 mia. til OWS, hvoraf størstedelen gik til BARDA og resten til forskning.23
HERAs har ikke et krisebudget at trække på ligesom BARDA. Det er derfor tvivlsomt, om nødhjælpsinstrumentet fremadrettet er tilstrækkeligt til at sikre, at HERA har adgang til den nødvendige risikovillige kapital i krisetider, da det er usikkert, hvor meget og hvor hurtigt EU kan mobilisere den nødvendige krisefinansiering. Situationen risikerer i hvert fald til forveksling at minde om Kommissionens indkøb af vacciner under coronakrisen. Her var en af forklaringerne på, at EU haltede efter USA og Storbritannien, at Kommissionen flere gange skulle bede medlemsstaterne om ekstra midler.24
Uden BARDA’s massive investeringer i nye teknologier og forskning i tidligere Covid-19 vira (dvs. MERS og SARS), havde det ikke været muligt at udrulle en Covid-19-vaccine på under et år. Som udtrykt af en repræsentant fra biotech-industrien, ”Vi var “heldige” med Covid-19. Vi kendte allerede til Spike proteinet i coronavira fra SARS og MERS, som USA har brugt millioner af dollars i at forske i det seneste årti. Det er derfor noget tvivlsomt, om man overhovedet kan kalde udviklingen af Covid-19-vaccinen en månelanding. USA har reddet os endnu engang. Næste gang der kommer en virus, kender vi den ikke nødvendigvis”.25
Massive investeringer i forskning og udvikling af medicinske modsvar i fredstid er alfa og omega for at imødegå fremtidige trusler hurtigt. Det er et område, hvor EU nu står stærkere med et robust beredskab i fredstid. Der er dog vigtigt at HERA har et direkte og dedikeret årligt budget, hvor det står klart, hvilke midler HERA kan regne med i beredskabsfasen. En stor del af HERA’s nuværende økonomiske midler kommer fra andre EU-programmer, hvor processen med at få adgang til og overført midlerne til HERA risikerer at blive bureaukratisk og langsom.
Dertil kommer, at EU’s syvårige budget er mejslet i sten og gør ikke EU særlig agil i krisetider. Som udtalt af professor Suerie Moon fra The Graduate Institute Geneva er, ”HERA ude af trit med EU’s budget, hvor der allerede er en på forhånd aftalt fast ramme for forskning og innovation. Måske skulle EU’s budget fungere anderledes. EU kunne oprette en reserve til at trække på i krisetider, ligesom den EU indførte for 15 år siden for veterinærkriser. Det er paradoksalt, at EU har en krisereserve for veterinærkriser, men ikke når kriser rammer mennesker [som f.eks. pandemier] ”.26 Medlemslandene og EU kunne med fordel trække på sine erfaringer med en krisereserve for veterinærkriser og lave en lignende løsning for alvorlige grænseoverskridende sundhedskriser. En mulig fremtidig finansieringsløsning er at give HERA en forhåndsgodkendt kreditbevilling til øjeblikkelig disposition – finansieret af medlemslandene – som er øremærket hasteudvikling og -produktion af medicinske modforanstaltninger. Det betyder, at medlemslandene forud for en krise har oprettet en reserve, som de kan trække på i krisetider.
For det andet er det vigtigt, at Kommissionen - ligesom under Covid-19-pandemien -investerer i forskellige typer teknologier, der kan noget forskelligt, dvs. satser bredt. I bagklogskabens klare lys fremstår EU’s forhandlingskrav til vaccineproducenter tilbage i 2020 om en lavere pris pr. dose dog som en tabersag. For hvorfor ikke bruge nogle ekstra milliarder euro på vacciner, når nedlukninger af de europæiske økonomier i den grad fik pengene til at fosse ud af statskasserne? Derfor bør HERA fremadrettet satse væsentligt i kroner og ører på flere heste.
For det tredje er embedsmænd i Kommissionen selv bekymret for, at ”HERA bliver endnu en bureaukratisk tjenestegren i Kommissionen, der skal koordinere mellem mange forskellige personer og enheder – og derfor risikerer ikke at have tilstrækkelig fokus på at eksekvere sine opgaver og være driftsklar”27 . Netop for HERA er det væsentligt at være driftsklar i forhold til alle sine opgaver – fra trusselsvurderinger og indsamling af efterretninger til fælles europæiske indkøb af medicinske modforanstaltninger. Det er særligt vigtigt i krisetid, at HERA kan agere hurtigt uden at skulle igennem en tung bureaukratisk koordineringsproces.
For det fjerde kan det være svært for HERA præcist at forudse, hvilke og hvor mange medicinske modforanstaltninger, EU har brug for at have på lager for at undgå unødigt spild af indkøbte lagerprodukter. Det er derfor vigtigt, at HERA indgår i tæt dialog med medlemsstaterne og deres eksperter for så præcist som muligt at få et billede af det reelle behov.
For det femte er det vigtigt, at HERA systematisk inddrager life science-industrien i alle dele af forsyningskæden i både beredskabs- og krisefasen. Gennem dialog med life science-industrien kan flere problemer tages i opløbet, som f.eks. at undgå, at markedet begynder at opføre sig irrationelt (så som hamstring af delkomponenter til produktionen). Derudover kan life science-industrien netop være med til at identificere markedsfejl ved at pege på de områder, hvor der mangler tilskyndelse til at forske i og investere i medicinske modforanstaltninger på trusler, virksomheder ikke selv er risikovillige til at investere i. For eksempel er antibiotikaresistens en stigende udfordring og et område virksomheder er mindre villige til at investere i pga. omkostninger forbundet med det. Lige nu er det usikkert, i hvilken grad industrien er inddraget i HERA’s beslutninger om R&D-støtte.
Sidst men ikke mindst er udvekslingen af nye datadelingsplatforme som det planlagte europæiske sundhedsdataområde en stor udfordring at få stablet på benene. Kommissionens planlagte forslag til et europæisk sundhedsdataområde i første kvartal af 2022 har til formål at fremme bedre udveksling af og adgang til forskellige typer sundhedsdata (så som elektroniske patientjournaler, genomdata, data fra patientregistre), der også kan anvendes til sundhedsforskning og sundhedspolitiske formål. Det vil indgå i både ECDC’s epidemiologiske overvågning og HERA’s trusselsovervågning. Det vil tage tid at opbygge de tre hovedsøjler i et fælles sundhedsdataområde, som udgør et robust system for datastyring og regler for dataudveksling, datakvalitet og en stærk infrastruktur og interoperabilitet. Det er tvivlsomt, om Kommissionen kan nå i mål med at implementere det inden 2025. Det skyldes, at EU ikke på nuværende tidspunkt har en fælles sundhedsdatainfrastruktur og få medlemslande har det på nationalt plan. HERA er dog ikke lige så afhængig af indikator-baseret manuel dataafrapportering fra medlemslandene, som ECDC er, indtil EU opnår en større digitalisering af sundhedsdataudveksling.
Disse problemområder gør, at EU kan blive udfordret, hvis/når der kommer en ny krise. Medlemsstaterne bør derfor være klar til at justere HERA’s struktur, der under alle omstændigheder kun er tænkt til at være midlertidig. Senest i 2024 skal Kommissionen udføre og forelægge en revision af den vedtagne rådsforordning om HERA’s krisekompetencer. Her skal Kommissionen særligt vurdere behovet for at oprette HERA som et selvstændigt agentur samt evaluere forholdet mellem HERA’s arbejde og indsats i beredskabs- og krisefasen.
Det er ikke givet, at et agentur vil give HERA flere beføjelser og større uafhængighed fra medlemslandene – om end det vil være mere uafhængigt af Kommissionen ved at blive placeret væk fra Kommissionen og have sin egen ledelse. Medlemslandene derimod spiller en stor rolle i de fleste af EU’s ca. 40 agenturer, hvor de gennem direkte repræsentation i bestyrelsen står for at udforme og godkende arbejdsprogrammer og -prioriteter. Et agentur uden de store muskler vil ikke nødvendigvis gøre HERA mere fleksibelt og agilt. Agenturer har dog typisk flere ansatte og flere finansielle midler, end HERA pt. har
Her og nu indtager medlemslandene og Kommissionen en ”vent og se”-holdning og lader HERA komme i gang. Der er stadig væsentlige mangler og uklarheder i HERA’s konstruktion (jf. tekstboks 2), som er vigtige at adressere fremadrettet for at sikre, at EU reelt står stærkere i fremtidige sundhedskriser.


- 1Europa-Kommissionen, Kommissionsformand Ursula von der Leyens tale om Unionens tilstand på Europa-Parlamentets plenarmøde, 16. september 2021, Bruxelles, tilgængelig her: ec.europa.eu/commission/presscorner/detail/da/SPEECH_20_1655 (besøgt 19. januar 2022).
- 2Dertil kom, at USA i modsætning til Europa indførte eksportrestriktioner, dvs. i lange periode nægtede at eksportere vacciner produceret inden for USA videre til andre, nødtrængende lande. Dette var en politik, der blev indledt af Præsident Trump og blev videreført af Præsident Biden.
- 3Dionigi, M.K. (2022). The ECDC – Challenges during and after the Covid-19-pandemic, Tænketanken Europa, 19. januar 2022, tilgængeligt her: thinkeuropa.dk/socialt/ecdc-challenges-during-and-after-covid-19-pandemic (besøgt 19. januar 2022).
- 4’HERA isn’t the hero Parliament wants – or the game-changer the Council fears’, Politico, 17. september 2021, tilgængelig her: www.politico.eu/article/hera-eu-commission-health-emergency-preparedness-response-authority/ (besøgt 19. januar 2022).
- 5Ibid
- 6For en samlet fremstilling af EU’s coronahåndtering fra krisens start til juni 2020, se Den europæiske improvisator, rapport af Tænketanken Europa, 24. juni 2021, tilgængelig her: thinkeuropa.dk/think/den-europaeiske-improvisator (besøgt 20. januar 2022).
- 7EU’s vaccinestrategi, Europa-Kommissionen, 17. juni 2020, tilgængelig her: ec.europa.eu/commission/presscorner/detail/en/ip_20_1103 (besøgt 20. januar 2022).
- 8Task Force for Industrial Scale-up of COVID-19 vaccines, Europa-Kommissionen, tilgængelig her: ec.europa.eu/growth/coronavirus-response/task-force-industrial-scale-covid-19-vaccines_da (besøgt 20. januar 2022).
- 9HERA Incubator to anticipate the threat of Covid-19 variants, Europa-Kommissionen, 17. januar 2021, tilgængelig her: ec.europa.eu/commission/presscorner/detail/en/AC_21_666 (besøgt 20. januar 2022).
- 10Europa-Kommissionen, Kommissionens afgørelse af 16. september 2021 om oprettelse af Myndigheden for Kriseberedskab og -indsats på Sundhedsområdet (2021/C 393 I/02), Den Europæiske Unions Tidende C 393 I/3, 29. september 2021, tilgængelig her: eur-lex.europa.eu/legal-content/DA/TXT/PDF/ (besøgt 20. januar 2022).
- 11Opening Remarks by Commissioner Stella Kyriakides during the exchange of views with the European Parliament ENVI Committee on HERA, 27. september 2021, Europa-Kommissionen, tilgængelig her: ec.europa.eu/commission/commissioners/2019-2024/kyriakides/announcements/opening-remarks-commissioner-kyriakides-during-exchange-views-european-parliament-envi-committee_en (besøgt 24. januar 2022).
- 12Ibid
- 13Europa-Kommissionen, Statsstøtte: Kommissionen vedtager reviderede statsstøtteregler for vigtige projekter af fælleseuropæisk interesse, pressemeddelelse, 25. november 2021, tilgængelig her: ec.europa.eu/commission/presscorner/detail/da/ip_21_6245 (besøgt 24. januar 2022).
- 14Rådets politiske enighed om en rådsforordning om en ramme for tiltag, der skal sikre forsyning af kriserelevante medicinske modforanstaltninger i tilfælde af en folkesundhedsmæssig krisesituation på EU-plan, Rådets generalsekretariat, 2021/0294 (NLE), 17. december 2021, tilgængelig her: data.consilium.europa.eu/doc/document/ST-15132-2021-INIT/en/pdf (besøgt 24. januar 2022).
- 15Europa-Parlamentet, Legislative Observatory, overblik over forhandlingerne af Kommissionens forslag til en forordning om alvorlige grænseoverskridende sundhedstrusler og om ophævelse af afgørelse nr. 1082/2013/EU, 2020/0322 (COD), tilgængelig her: oeil.secure.europarl.europa.eu/oeil/popups/ficheprocedure.do (besøgt 24. januar 2022).
- 16Et mellemstatsligt udvalg under Kommissionen med tekniske sundhedsfaglige repræsentanter fra alle EU’s medlemslande. Udvalget har mandat til at styrke koordineringen og udvekslingen af bedste praksis og oplysninger om nationale beredskabsaktiviteter. Medlemslandene rådfører sig med hinanden i udvalget med henblik på at koordinere de nationale reaktioner på alvorlige grænseoverskridende sundhedstrusler.
- 17Anonymt interview med rådsrepræsentant, 24. januar 2022.
- 18Anonymt interview med kommissionsembedsmand, 26. januar 2022.
- 19Rådets forordning (EU) 2016/369 af 15. marts 2016 om ydelse af nødhjælp i Unionen, tilgængelig her: eur-lex.europa.eu/legal-content/DA/TXT/PDF/ (besøgt 24. januar 2022).
- 20Europa-Kommissionens indledende konsekvensanalyse om HERA, Ref. Ares (2021)674649, d. 27. januar 2021, tilgængelig her: ec.europa.eu/info/law/better-regulation/have-your-say/initiatives/12870-European-Health-Emergency-Preparedness-and-Response-Authority-HERA-_en (besøgt 24. januar 2022).
- 21Europa-Parlamentets holdning i første behandling af forslaget om forordning om alvorlige grænseoverskridende sundhedstrusler og om ophævelse af afgørelse nr. 1082/2013/EU, 11. november 2021, tilgængelig her: www.europarl.europa.eu/doceo/document/TA-9-2021-0449_EN.pdf (besøgt 24. januar 2022).
- 22Europa-Kommissionen, EU’s vaccinestrategi, tilgængelig her: ec.europa.eu/info/live-work-travel-eu/coronavirus-response/public-health/eu-vaccines-strategy_da (besøgt 24. januar 2022).
- 23Kirkegaard, J. F. (2021). The European Union’s troubled COVID-19 vaccine rollout, PIIE, 15. marts 2021, tilgængelig her: www.piie.com/blogs/realtime-economic-issues-watch/european-unions-troubled-covid-19-vaccine-rollout (besøgt 24. januar 2022).
- 24Friis, L. & Schmidt, J.H. (2020). Fra EU’s vaccinestrategi til det globale vaccinediplomati, 16. januar 2021, tilgængelig her: thinkeuropa.dk/sites/default/files/final_notat_vaccine_0.pdf (besøgt 19. januar 2022).
- 25Anonymt interview med repræsentant for en biotech-virksomhed, 6. december 2021.
- 26Præsentation af Prof. Suerie Moon, direktør ved Global Health Centre ved The Graduate Institute Geneva, CEPS Ideas Lab, Towards a European Health Union, 31. maj 2021, tilgængelig her: www.youtube.com/watch (besøgt 19. januar 2022).
- 27Anonymt interview med kommissionsembedsmand, 26. januar 2022.
Tænketanken EUROPA indtager ikke holdninger som organisation. Denne tekst repræsenterer alene – som alle udgivelser fra Tænketanken EUROPA – forfatterens/forfatternes betragtninger.



